IA Générative en Santé : 5 Cas d'Usage Validés + Conformité 2026

Ikasia, cabinet de conseil IA et formation IA basé à Paris, accompagne les établissements de santé français dans l'adoption de l'intelligence artificielle générative. Ce guide couvre les cas d'usage validés en 2026 — documentation clinique, aide au diagnostic, recherche pharmaceutique — ainsi que les exigences réglementaires (AI Act, MDR, RGPD) spécifiques au secteur médical.
En bref : L'IA générative en santé entre en production en 2026 : documentation clinique (réduction significative du temps), aide au diagnostic, accélération pharma. Cadre réglementaire triple (AI Act + MDR + RGPD). L'humain reste décisionnaire.
Le secteur de la santé connaît une révolution silencieuse. L'IA générative, longtemps cantonnée aux POCs, entre en production dans les établissements de santé : documentation clinique automatisée, aide au diagnostic, accélération de la recherche pharmaceutique. Mais ce secteur ultra-réglementé impose des contraintes spécifiques. Comment déployer l'IA générative en santé de manière sûre et conforme ?
L'IA générative en santé : Panorama des cas d'usage 2026
État des lieux du marché
L'IA en santé représente un marché en forte croissance, estimé à plusieurs dizaines de milliards de dollars en 2025 avec une croissance annuelle supérieure à 30 % selon les cabinets d'analyse.
Principaux segments (par ordre d'importance) :
- Diagnostic assisté
- Documentation clinique
- Découverte de médicaments
- Administration et gestion
- Monitoring patients
Les 6 cas d'usage majeurs de l'IA générative en santé
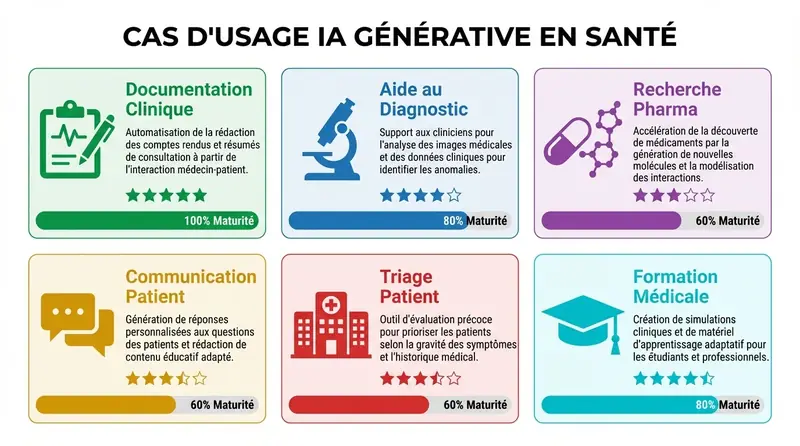
Documentation clinique : Réduire la charge administrative
Le problème
Les médecins passent en moyenne 2 heures de documentation pour 1 heure de soin patient. Cette charge administrative est une cause majeure de burnout et de désengagement.
La solution : Ambient Clinical Intelligence
L'IA générative écoute la consultation (avec consentement patient) et génère automatiquement :
- Le compte-rendu de consultation
- Les prescriptions à valider
- Les codes diagnostics (CIM-10, CCAM)
- La lettre au médecin traitant
Exemple : DAX Copilot de Nuance/Microsoft
Déployé dans plusieurs CHU français depuis 2025 :
Processus :
1. Le médecin active l'enregistrement (consentement patient)
2. La consultation se déroule normalement
3. DAX transcrit et structure en temps réel
4. Le médecin valide/corrige le CR généré
5. Intégration automatique au DPI (Dossier Patient Informatisé)
Résultats observés :
- Temps de documentation : une réduction significative
- Satisfaction médecins : en nette hausse
- Complétude des CR : une amélioration notable
- Erreurs de codage : une diminution des erreurs de codage
Points d'attention
- Consentement patient : Obligatoire et documenté
- Validation humaine : Le médecin reste responsable
- Intégration DPI : Complexe selon les éditeurs (Dedalus, Maincare, etc.)
- Langue française : Performances variables selon les accents et jargons
Aide au diagnostic : LLMs comme second avis médical
Le concept
Les LLMs peuvent analyser les symptômes, l'historique patient et les examens pour suggérer des diagnostics différentiels. Ils ne remplacent pas le médecin mais enrichissent sa réflexion.
Cas d'usage 1 : Analyse d'imagerie médicale
Radiologie (scanner, IRM, radio) :
- Détection d'anomalies (nodules, fractures, AVC)
- Priorisation des urgences
- Mesures automatiques (taille tumeurs, volumes)
Dermatologie :
- Classification des lésions cutanées
- Détection précoce mélanome
- Suivi évolutif
Ophtalmologie :
- Rétinopathie diabétique
- DMLA
- Glaucome
Cas d'usage 2 : Synthèse du dossier patient
Le LLM synthétise l'ensemble du dossier patient pour :
- Identifier les antécédents pertinents
- Détecter les interactions médicamenteuses
- Alerter sur les contre-indications
Exemple de prompt médical :
Tu es un assistant médical. Analyse ce dossier patient et fournis :
1. Résumé des antécédents significatifs
2. Médicaments en cours et interactions potentielles
3. Alertes sur les examens manquants selon les recommandations HAS
4. Questions à poser au patient
Patient : [données anonymisées]
Cas d'usage 3 : Diagnostic différentiel
Workflow typique :
Symptômes + Examens + Antécédents
↓
LLM médical
↓
Liste de diagnostics possibles
(avec probabilités estimées)
↓
Médecin évalue et décide
Limites et précautions
Ce que l'IA NE PEUT PAS faire :
- Poser un diagnostic définitif
- Prescrire un traitement
- Remplacer l'examen clinique
- Gérer les cas atypiques
Risques identifiés :
- Biais d'automation : Sur-confiance dans l'IA
- Hallucinations : Diagnostics inventés — les approches RAG vs fine-tuning permettent de réduire ce risque
- Biais de données : Sous-représentation de certaines populations
- Responsabilité : Qui est responsable en cas d'erreur ?
Recherche pharmaceutique : Accélération des découvertes
Le contexte
Développer un médicament prend 10-15 ans et coûte 2-3 milliards USD en moyenne. L'IA générative peut accélérer plusieurs étapes.
Applications de l'IA générative en pharma
1. Génération de molécules candidates Les modèles génératifs (diffusion models, GNNs) proposent des structures moléculaires optimisées pour une cible thérapeutique.
2. Prédiction de toxicité Avant la synthèse, l'IA prédit la toxicité potentielle et filtre les candidats dangereux.
3. Optimisation des essais cliniques
- Sélection des patients (critères d'inclusion)
- Prédiction des abandons
- Détection des effets secondaires
4. Analyse de la littérature scientifique LLMs analysent des millions d'articles pour identifier :
- Nouvelles cibles thérapeutiques
- Repositionnement de médicaments existants
- Tendances de recherche
Exemple : AlphaFold et la biologie structurale
DeepMind's AlphaFold a révolutionné la prédiction de structure des protéines :
- Base de données de 200 millions de structures prédites
- Un gain de temps considérable pour certaines étapes de recherche
- Applications en développement de médicaments, agriculture, environnement
Exigences AI Act pour les dispositifs médicaux IA
Classification des systèmes IA en santé
L'AI Act européen classe les systèmes IA médicaux principalement en risque élevé :
Systèmes à risque élevé (Annexe III) :
- Dispositifs médicaux (classes IIa et supérieures selon MDR)
- Systèmes d'aide au diagnostic
- Systèmes influençant les décisions de traitement
- Outils de triage aux urgences
Obligations spécifiques :
| Obligation | Détail |
|---|---|
| Système de gestion des risques | Identification, évaluation, mitigation des risques |
| Gouvernance des données | Qualité, représentativité, traçabilité des datasets |
| Documentation technique | Description complète du système |
| Transparence | Information des utilisateurs sur les capacités/limites — voir notre article sur l'IA explicable (XAI) et la transparence |
| Supervision humaine | Possibilité d'override humain |
| Précision et robustesse | Tests de performance documentés |
| Cybersécurité | Protection contre les attaques |
Articulation AI Act / MDR
Le règlement européen sur les dispositifs médicaux (MDR 2017/745) s'applique EN PLUS de l'AI Act :
Un système IA médical est soumis à trois cadres réglementaires simultanés :
- AI Act (si IA) -- Obligations risque élevé
- MDR (si dispositif médical) -- Marquage CE, évaluation clinique
- RGPD (si données personnelles) -- Base légale, droits patients
Calendrier de conformité
| Date | Obligation |
|---|---|
| Février 2025 | Pratiques interdites + littératie IA |
| Août 2025 | Obligations GPAI |
| Août 2026 | Obligations complètes risque élevé |
| Août 2027 | Dispositifs médicaux IA (classe IIa+) |
RGPD et données de santé : Le cadre juridique spécifique
Les données de santé sont des données sensibles
Le RGPD (article 9) interdit par principe le traitement des données de santé, sauf exceptions :
- Consentement explicite du patient
- Nécessité pour les soins
- Intérêt public en santé publique
- Recherche scientifique (avec garanties)
Base légale pour l'IA médicale
En contexte de soins :
- Base légale : Exécution d'une mission d'intérêt public + nécessité pour les soins
- Pas de consentement requis pour le soin lui-même
- MAIS information claire du patient sur l'utilisation de l'IA
En contexte de recherche :
- Base légale : Intérêt public en recherche scientifique
- Avis CNIL/Comité éthique requis
- Pseudonymisation ou anonymisation nécessaire
Droits des patients
| Droit | Application IA médicale |
|---|---|
| Information | Savoir qu'une IA est utilisée |
| Accès | Obtenir les données utilisées |
| Rectification | Corriger les erreurs |
| Opposition | Refuser l'utilisation de l'IA pour ses soins |
| Explication | Comprendre la logique de la décision IA |
| Intervention humaine | Demander une décision humaine |
Focus : Le Health Data Hub
Le Health Data Hub (HDH) centralise les données de santé françaises pour la recherche :
- Accès encadré pour les projets de recherche
- Procédure d'autorisation CNIL
- Environnement sécurisé d'analyse
Utilisation pour l'IA :
- Entraînement de modèles sur données réelles
- Validation sur cohortes françaises
- Benchmark national des performances
Déployer l'IA en milieu médical : Méthodologie
Phase 1 : Qualification réglementaire (2-4 mois)
Questions clés :
- L'outil est-il un dispositif médical au sens MDR ?
- Quelle classe de risque AI Act ?
- Quelles données sont traitées ?
Livrables :
- Analyse réglementaire documentée
- Stratégie de conformité
- Budget et timeline
Phase 2 : Évaluation clinique (3-6 mois)
Objectifs :
- Démontrer la sécurité clinique
- Mesurer les performances réelles
- Identifier les biais et limites
Méthode :
1. Définir les critères de performance (sensibilité, spécificité, etc.)
2. Constituer un dataset de test représentatif
3. Évaluation prospective sur cas réels
4. Analyse des erreurs et ajustements
5. Documentation complète
Phase 3 : Intégration technique (2-4 mois)
Points d'attention :
- Interopérabilité DPI (HL7 FHIR, IHE)
- Authentification forte (carte CPS, Pro Santé Connect) — la sécurisation des LLMs est un prérequis
- Hébergement HDS (Hébergeur de Données de Santé)
- Traçabilité des accès
Phase 4 : Conduite du changement (ongoing)
Les freins côté soignants :
- Méfiance envers la technologie
- Peur du remplacement
- Charge de travail perçue pour la transition
Leviers d'adoption :
- Impliquer les soignants dès la conception
- Former sur les bénéfices concrets (gain de temps)
- Rassurer sur le rôle de validation humaine
- Mesurer et communiquer les résultats
Phase 5 : Surveillance post-déploiement
Obligations MDR/AI Act :
- Monitoring continu des performances
- Signalement des incidents
- Mise à jour régulière du système
- Audit périodique
Étude de cas : Déploiement IA documentation CHU
Contexte
Un CHU de 2500 lits souhaite déployer l'IA de documentation clinique.
Approche
Mois 1-2 : Cadrage
- Audit réglementaire : Dispositif médical classe I
- Choix de solution : DAX Copilot (Microsoft/Nuance)
- Constitution équipe projet (médecins, DSI, DPO, juriste)
Mois 3-4 : Pilote
- 20 médecins volontaires (3 services)
- Formation initiale (4h)
- Évaluation continue qualité/satisfaction
Mois 5-6 : Évaluation
- Analyse des CR générés (qualité, complétude)
- Mesure temps gagné
- Retours utilisateurs
- Ajustements workflow
Mois 7-12 : Déploiement progressif
- Extension par vagues (50 → 150 → 500 médecins)
- Formation des formateurs internes
- Communication institutionnelle
Résultats
| Métrique | Avant | Après | Évolution |
|---|---|---|---|
| Temps documentation/patient | 15 min | 7 min | -53% |
| Satisfaction médecins (NPS) | 12 | 47 | +35 pts |
| Complétude CR | 72% | 91% | +19 pts |
| Erreurs codage | 8% | 5% | -3 pts |
Notre accompagnement IA Santé
Chez Ikasia, nous accompagnons les établissements de santé :
Audit IA Santé (3 jours)
- Cartographie des cas d'usage pertinents
- Analyse réglementaire (MDR, AI Act, RGPD)
- Roadmap de déploiement
Formation "IA pour professionnels de santé" (1 jour)
- Comprendre les capacités et limites de l'IA
- Cas pratiques médicaux
- Enjeux éthiques et réglementaires
Accompagnement projet IA médicale (3-12 mois)
- Pilotage projet complet
- Conformité réglementaire
- Conduite du changement
Conclusion
L'IA générative transforme la santé de manière tangible en 2026 : documentation clinique automatisée, aide au diagnostic, accélération de la recherche. Mais ce secteur ultra-réglementé impose une approche rigoureuse.
Les clés du succès :
- Commencer par la documentation clinique : ROI rapide, risque maîtrisé — notre guide pour intégrer l'IA en entreprise détaille la méthodologie
- Anticiper la conformité : AI Act + MDR + RGPD = complexité réglementaire
- Impliquer les soignants : L'adoption dépend de leur engagement
- Garder l'humain au centre : L'IA assiste, le médecin décide
Le potentiel est immense : réduire la charge administrative, améliorer la qualité diagnostique, accélérer les découvertes thérapeutiques. Mais seules les organisations qui maîtrisent à la fois la technologie ET la réglementation en tireront les bénéfices.
Cet article vous a intéressé ? Découvrez notre Atelier IA Générative — 3h30 hands-on pour maîtriser l'outil en équipe.
Tags
Formations associées
Articles similaires

IA en santé : conformité DGS, HAS et CE marking des dispositifs médicaux (guide 2026)
Lire
Checklist RGPD et IA : 10 points à vérifier avant de déployer un outil d'intelligence artificielle
Lire
IA générative et propriété intellectuelle : ce que les juristes d'entreprise doivent savoir en 2026
LireEnvie d'aller plus loin ?
Ikasia propose des formations IA conçues pour les professionnels. De la stratégie aux ateliers techniques pratiques.